Blog
Aligned Elements is a Medical Device application lifecycle management (ALM) solution enabling fast development and regulatory compliance through improved Design History File management.
Traceability
-
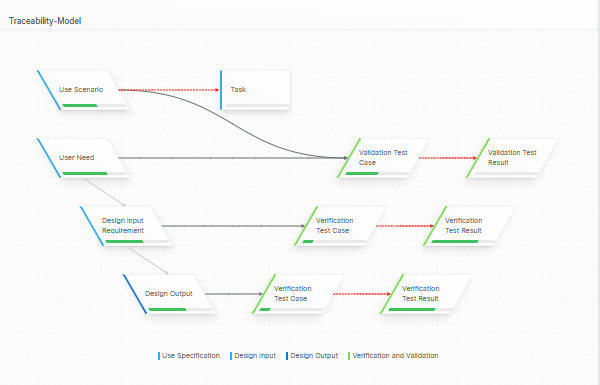
Traceability Management: Der Motor Ihres Designs
Die Definition der Rückverfolgbarkeitsstruktur Ihrer Design-Steuerungen ist die wertvollste, strategische Maßnahme in der Frühphase. Diese Struktur ist der Motor, der Ihre Entwicklung vorantreibt, Lücken im Design sofort aufdeckt und Ihnen letztendlich ein vollständiges, konsistentes und korrektes Technical File liefert.
Lassen Sie Aligned Elements Ihre Traceability-Matrizen erstellen, die exakt auf Standards wie IEC 62304, IEC 62366 und ISO 14971 sowie auf Ihrem eigenen Qualitätssystem und Ihren Entwicklungs-SOPs zugeschnitten sind.
Halten Sie Ihre Rückverfolgbarkeit vollständig und konsistent, während Sie sich voll auf das Design selbst konzentrieren.
-
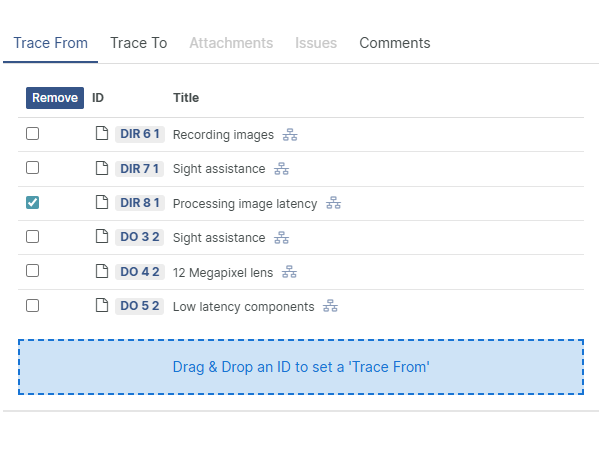
Live-Rückverfolgbarkeit – Immer griffbereit
Das Setzen von Traces muss sich einfach anfühlen. Egal, wo Sie sich im Projekt befinden, die Trace-Aktionen sind sofort verfügbar – kein lästiges Wechseln von Ansichten oder unnötige Schritte.
Ob Sie Elemente per Drag-and-Drop verknüpfen, aus
intelligenten Suchlisten auswählen oder in einem Schritt erstellen und verknüpfen: alles ist darauf ausgelegt, schnell und reibungslos zu sein.Sie können Fehler beheben und Verknüpfungen im selben Arbeitsschritt setzen, Stapeländerungen über große Mengen anwenden und Verknüpfungen nahtlos über mehrere Projekte hinweg verwalten.
Wenn Rückverfolgbarkeit so einfach ist, bedeutet dies weniger Unterbrechungen, weniger übersehene Verknüpfungen und ein enormes Plus an Vertrauen in Ihre Daten.
-
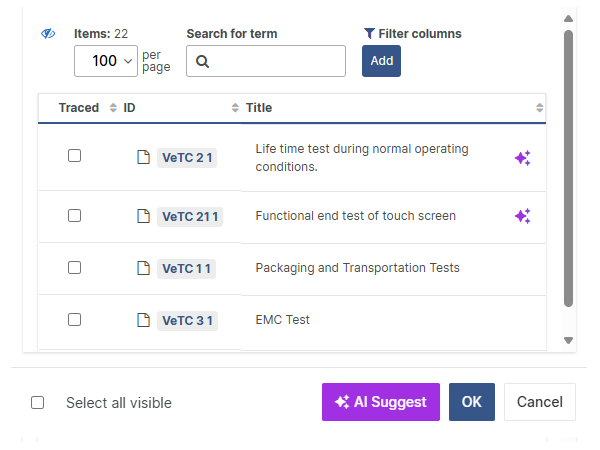
Entdecken Sie KI-gesteuerte Trace-Kandidaten
Gerade bei großen Medizinprodukte-Projekten mit Tausenden von Verknüpfungen erhöht das schiere Ausmaß das Risiko, relevante Verbindungen unbeabsichtigt zu übersehen.
Mit KI-gestützter Unterstützung können Sie die von unserer KI vorgeschlagenen Trace-Kandidaten mit Ihrer eigenen Auswahl erkunden und vergleichen. Sie behalten dabei stets die volle Kontrolle und treffen immer die endgültige Entscheidung.
Dennoch erhalten Sie die Unterstützung eines "zweiten Augenpaares", das darauf trainiert ist, übersehene Kandidaten aufzudecken. Egal, ob Sie bei null beginnen oder bestehende Rückverfolgbarkeit überprüfen: Unsere KI bietet Ihnen die Möglichkeit, Ihre Arbeit in Echtzeit mit intelligenten, kontextbasierten Vorschlägen abzugleichen.
-
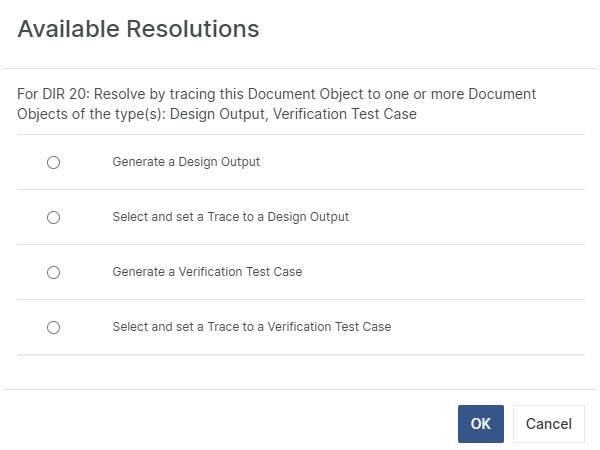
Trace-Fehler – In Sekunden erkannt und gelöst
Eliminieren Sie Rückverfolgbarkeitsfehler mithilfe unserer integrierten Impact Analysis, um die Auswirkungen von Änderungen im aktuellen Projektkontext sofort zu verstehen.
Führen Sie kontinuierliche Echtzeit Konsistenzprüfungen durch, um Lücken zu erkennen, und nutzen Sie die Trace Analysis jederzeit, um fehlende, illegale, verdächtige oder veraltete Verknüpfungen zu identifizieren.
Das Beste: Sie wählen aus den von Aligned Elements vorgeschlagenen Lösungen und beheben das Problem mit nur einem einzigen Klick.
Das Erkennen von Rückverfolgbarkeitsproblemen und die Ergreifung von Maßnahmen zu deren Lösung war noch nie einfacher und unkomplizierter.
-

Schnelle und flexible Generierung von Traceability-Matrizen
Erstellen Sie Ihre eigenen, kundenspezifischen Trace Tables und Matrizen on-the-fly im integrierten Trace Table Designer.
Die Generierung einer vollständigen End-to-End-Trace-Tabelle, basierend auf Ihrem individuellen Design, ist innerhalb von Sekunden abgeschlossen.
Überprüfen Sie die Ergebnisse, nehmen Sie bei Bedarf Änderungen am Design vor oder gehen Sie direkt zur Veröffentlichung der relevanten Dokumente über.
Sie exportieren die Rückverfolgbarkeitsmatrix nach Word oder Excel oder fügen sie direkt in Ihre Technical File Documents ein, indem Sie unser einzigartiges Word Add-In verwenden.
Ein einziger Klick genügt, um Ihre Dokumente, die Traceability-Matrizen enthalten, zu aktualisieren und sie mit den allerneuesten Rückverfolgbarkeitsinformationen zu befüllen.
Ohne Umwege zur CE Kennzeichnung und FDA Zulassung
Testen Sie Aligned Elemente kostenlos für 30 Tage!
Echte Stimmen, greifbare Ergebnisse
Echte Stimmen, greifbare Ergebnisse
